انسان بدون وجود نداشت ویروس ها زیرا پروتئین ویروسی نقش کلیدی در ایجاد انسان جنین با این حال، گاهی اوقات، آنها تهدیدات وجودی را در قالب بیماری ایجاد می کنند، مانند مورد همه گیری فعلی COVID-19. از قضا، ویروس ها حدود 8 درصد از ژنوم ما را تشکیل می دهد که در طول سیر تکامل به دست آمده است و ما را تقریباً یک واهی می سازد.
بدنام ترین و وحشتناک ترین کلمه سال 2020 بدون شک این استویروس'. رمان قرنطینه مسئول بیماری بیسابقه کووید-19 فعلی و تقریباً سقوط اقتصاد جهانی است. همه اینها توسط یک ذره کوچک ایجاد می شود که حتی به عنوان "کاملا" زنده در نظر گرفته نمی شود زیرا در یک حالت غیرعملکردی در خارج از میزبان قرار دارد، در حالی که تنها با آلوده کردن میزبان در داخل تداوم می یابد. شگفتانگیزتر و تکاندهندهتر این واقعیت است که انسان از زمانهای بسیار قدیم حامل "ژنهای" ویروسی بودهاند و در حال حاضر ژنهای ویروسی حدود 8 درصد از ژنهای ویروسی را تشکیل میدهند. انسان ژنوم (1). فقط برای در نظر گرفتن این موضوع، فقط 1٪ انسان ژنوم از نظر عملکردی مسئول ساخت پروتئین هایی است که تعیین می کنند ما چه کسی هستیم.
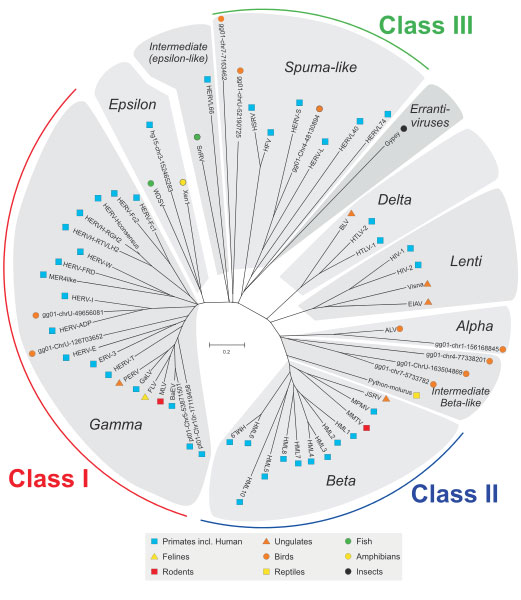
داستان رابطه بین انسان و ویروس ها 20-100 میلیون سال پیش زمانی که اجداد ما آلوده شدند شروع شد ویروس ها. هر خانواده رتروویروس درون زا از یک عفونت منفرد سلول های زایا توسط یک رتروویروس اگزوژن مشتق شده است که پس از ادغام در جد ما، گسترش یافته و تکامل یافته است (2). انتشار و به دنبال آن انتقال افقی از والدین به فرزندان و امروزه ما این ژنوم های ویروسی را در DNA خود جای داده ایم. انسان رتروویروس های درون زا (HERVs). این یک روند مستمر است و حتی ممکن است در حال حاضر اتفاق بیفتد. در طول تکامل، این HERV ها جهش هایی به دست آوردند و در آن تثبیت شدند انسان ژنوم و توانایی خود را برای ایجاد بیماری از دست دادند. درون زا ویروسهای ویروس نه تنها در انسان اما در همه موجودات زنده وجود دارند. همه این رتروویروسهای درونزا که در سه کلاس (کلاس I، II و III) گروهبندی شدهاند، در گونههای مختلف جانوری یک رابطه فیلوژنتیکی بر اساس شباهت توالی آنها (3) نشان میدهند که در شکل زیر نشان داده شده است. HERV ها متعلق به گروه کلاس I هستند.
از رتروویروسهای تعبیهشده مختلف موجود در انسان ژنوم، یک مثال کلاسیک که در اینجا قابل ذکر است، ژنوم یک پروتئین رتروویروسی است که پروتئین پوششی بسیار همجوشی به نام سینسیتین است، (5) که عملکرد اصلی آن در ویروس برای ایجاد عفونت با سلول های میزبان ترکیب شد. این پروتئین در حال حاضر سازگار شده است انسان برای تشکیل جفت (ادغام سلول ها برای ساخت سلول های چند هسته ای) که نه تنها غذای جنین را از مادر در دوران بارداری تامین می کند، بلکه به دلیل ماهیت سرکوب کننده سیستم ایمنی پروتئین سینسیتین، از جنین در برابر سیستم ایمنی مادر محافظت می کند. ثابت شده است که این HERV خاص برای افراد مفید است انسان نژاد با تعریف وجود خود.
HERV ها همچنین در ایجاد ایمنی ذاتی برای میزبان با جلوگیری از عفونت بیشتر مربوطه نقش دارند. ویروس ها یا کاهش شدت بیماری در صورت عفونت مجدد توسط نوع مشابه ویروس ها. یک بررسی در سال 2016 توسط کاتزوراکیس و اسود (6) آن درون زا را توصیف می کند. ویروس ها می تواند به عنوان عناصر تنظیم کننده برای ژن هایی عمل کند که عملکرد ایمنی را کنترل می کنند و در نتیجه منجر به توسعه ایمنی می شود. در همان سال، چونگ و همکاران (7) نشان دادند که برخی از HERV ها با تعدیل بیان ژن های القایی IFN (اینترفرون) به عنوان تقویت کننده های تنظیمی عمل می کنند و در نتیجه ایمنی ذاتی ایجاد می کنند. محصولات بیان HERV همچنین میتوانند بهعنوان الگوهای مولکولی مرتبط با بیماریزا (PAMPs) عمل کنند و گیرندههای سلولی مسئول خط اول دفاع میزبان را تحریک کنند (8-10).
یکی دیگر از جنبه های جالب HERV ها این است که برخی از آنها پلی مورفیسم های درج را نشان می دهند، یعنی تعداد متفاوتی از کپی ها در ژنوم به دلیل رویدادهای درج وجود دارد. مطالعه بر روی 20 آزمودنی متعلق به گروه های قومی مختلف، الگوهای چندشکلی درج را بین 0 تا 87 درصد در همه افراد نشان داد (11). این می تواند پیامدهایی در ایجاد بیماری با فعال شدن ژن های خاصی داشته باشد که در غیر این صورت خاموش هستند.
همچنین نشان داده شده است که برخی از HERV ها با ایجاد اختلالات خودایمنی مانند مولتیپل اسکلروزیس مرتبط هستند (12). در شرایط فیزیولوژیکی طبیعی، بیان HERV به شدت تنظیم می شود در حالی که در شرایط پاتولوژیک به دلیل تغییرات در محیط خارجی/داخلی، تغییرات هورمونی و/یا تعامل میکروبی می تواند باعث اختلال در بیان HERV شود که منجر به بیماری شود.
ویژگی های فوق HERV نشان می دهد که نه تنها حضور آنها در انسان ژنوم اجتناب ناپذیر است، اما آنها توانایی تنظیم هموستاز سیستم ایمنی را یا با فعال کردن یا سرکوب آن دارند، در نتیجه باعث ایجاد اثرات متفاوت (از مفید بودن تا ایجاد بیماری) در میزبان می شوند.
همهگیری COVID-19 همچنین توسط یک رتروویروس SARS-nCoV-2 ایجاد میشود که به خانواده آنفولانزا تعلق دارد، و ممکن است قابل قبول باشد که در طول سیر تکامل، ژنومهای مربوط به این خانواده از ویروس ها در ادغام شد انسان ژنوم و اکنون به عنوان HERV وجود دارد. فرض بر این است که این HERV ها ممکن است پلی مورفیسم های مختلفی را، همانطور که در بالا ذکر شد، در بین افراد قومیت های مختلف نشان دهند. این پلیمورفیسمها ممکن است به صورت تعداد کپی دیفرانسیل این HERVها و/یا وجود یا عدم وجود جهشها (تغییرات در توالی ژنوم) در یک دوره زمانی انباشته شده باشند. این تنوع در HERV های یکپارچه ممکن است توضیحی برای نرخ های متفاوت مرگ و میر و شدت بیماری COVID-19 در کشورهای مختلف تحت تأثیر این همه گیری ارائه دهد.
***
منابع:
1. Griffiths DJ 2001. رتروویروس های درون زا در انسان توالی ژنوم ژنوم بیول. (2001)؛ 2 (6) نظرات 1017. DOI: https://doi.org/10.1186/gb-2001-2-6-reviews1017
2. Boeke, JD; استوی، جی پی (1997). "رتروترانسپوزون ها، رتروویروس های درون زا، و تکامل عناصر رتررو". در تابوت، JM; هیوز، SH; وارموس، HE (ویرایشگران). رتروویروس ها مطبوعات آزمایشگاهی Cold Spring Harbor. PMID 21433351.
3. Vargiu L، و همکاران. طبقه بندی و خصوصیات انسان رتروویروس های درون زا؛ اشکال موزاییک رایج است. Retrovirology (2016); 13: 7. DOI: 10.1186 / s12977-015-0232-y
4. Classes_of_ERVs.jpg: Jern P, Sperber GO, Blomberg J (کار مشتق شده: Fgrammen (گفتگو))، 2010. در دسترس آنلاین در https://commons.wikimedia.org/wiki/File:Classes_of_ERVs.svg مشاهده شده در 07 مه 2020
5. بلوند، جی ال. لاویلت، دی. Cheynet، V; بوتون، O; اوریول، جی. چپل-فرناندز، اس. مانداندس، اس. مالت، F; Cosset، FL (7 آوریل 2000). گلیکوپروتئین پاکتی از انسان درونی رتروویروس HERV-W در جفت انسان بیان می شود و سلول هایی را که گیرنده رتروویروس پستانداران نوع D را بیان می کنند ترکیب می کند. جی. ویرول. 74 (7): 3321-9. DOI: https://doi.org/10.1128/jvi.74.7.3321-3329.2000.
6. Katzourakis A، و Aswad A. تکامل: درون زا ویروس ها ایجاد میانبر در ایمنی ضد ویروسی زیست شناسی فعلی (2016). 26: R427-R429. http://dx.doi.org/10.1016/j.cub.2016.03.072
7. Chuong EB، Elde NC، و Feschotte C. تکامل تنظیمی ایمنی ذاتی از طریق انتخاب رتروویروس های درون زا. علوم (2016) جلد. 351، ش 6277، ص 1083-1087. DOI: https://doi.org/10.1126/science.aad5497
8. Wolff F، Leisch M، Greil R، Risch A، Pleyer L. شمشیر دولبه بیان (دوباره) ژن ها توسط عوامل هیپومتیل کننده: از تقلید ویروسی تا بهره برداری به عنوان عوامل آغازگر برای مدولاسیون هدفمند ایست بازرسی ایمنی. سیگنال ارتباط سلولی (2017) 15:13. DOI: https://doi.org/10.1186/s12964-017-0168-z
9. Hurst TP، Magiorkinis G. فعال شدن پاسخ ایمنی ذاتی توسط درون زا ویروسهای ویروس. جی ژنر ویرول. (2015) 96:1207-1218. DOI: https://doi.org/10.1099/vir.0.000017
10. Chiappinelli KB، Strissel PL، Desrichard A، Chan TA، Baylin SB، Correspondence S. مهار متیلاسیون DNA باعث پاسخ اینترفرون در سرطان از طریق dsRNA از جمله رتروویروس های درون زا می شود. Cell (2015) 162:974-986. DOI: https://doi.org/10.1016/j.cell.2015.07.011
11. مهراب جی، سیبل ی، کانیه اس، سوگی م و نرمین جی. درون زا انسانی رتروویروسغربالگری درج H. گزارش های پزشکی مولکولی (2013). DOI: https://doi.org/10.3892/mmr.2013.1295
12. Gröger V و Cynis H. رتروویروس های درون زا انسانی و نقش احتمالی آنها در ایجاد اختلالات خود ایمنی مانند مولتیپل اسکلروزیس. میکروبیول جلو. (2018)؛ 9: 265. DOI: https://doi.org/10.3389/fmicb.2018.00265
***